
Una investigación llevada a cabo por científicos de la Universidad Técnica de Delf (Países Bajos) y el laboratorio de Margarita Salas en el Centro de Biología Molecular Severo Ochoa, centro de la Universidad Autónoma de Madrid y el CSIC, ha logrado desarrollar un minigenoma que se replica. Utilizando el virus bacteriano Phi29, han conseguido que un minigenoma exprese las proteínas que lo replican una y otra vez, lo cual es un nuevo paso hacia la creación de una célula artificial.
Cabe indicar que el ensamblaje de la primera célula sintética es un reto de la biología actual, al que los científicos apenas han conseguido acercarse. Alcanzarlo no solo pondría a prueba la ciencia que damos por sentada hoy en día, sino que también podría abrir toda una serie de posibilidades, tanto a nivel de conocimiento como de aplicaciones prácticas.
Para construir una célula artificial o sintética, son muchos los sistemas que tienen que funcionar a la perfección y estar coordinados. Conocemos más o menos cómo funcionan los componentes de la célula por separado, pero al ponerlos a funcionar todos a la vez, la complejidad supera nuestro actual conocimiento.
Sin embargo, hay una serie de pilares desde los que se puede construir. Por un lado, una de las funciones claves a incluir en una célula artificial, es la replicación del material genético. Y por otro, se necesita que dicho material genético se exprese, y la forma en que lo hace, es a través de la producción de un mensajero (el mRNA), siendo necesarias proteínas que hagan que se cumplan las instrucciones de ese mensaje. Finalmente, sería necesaria una membrana que separe la célula del exterior.
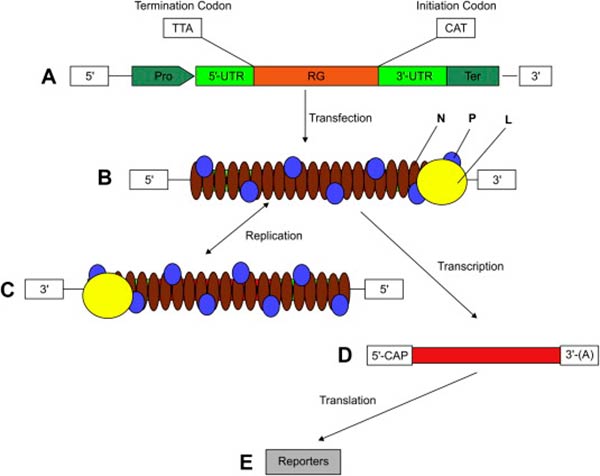
En este contexto, el trabajo en equipo de dichos científicos, logró crear un minigenoma que se replica en un tubo de ensayo. Estos resultados, publicados en Nature Communications, demuestran la posibilidad de imitar la función de replicación de material genético, lo que significa un paso importante en la dirección de construir la primera célula sintética, según los autores.
Para conseguir esto, el equipo ha implementado la maquinaria de replicación de ADN del virus Phi29 en un sistema de expresión génica sin células. El laboratorio de Christophe Danelon en Delft, se ha centrado en el problema de poner en funcionamiento este sistema mínimo o minigenoma in vitro y que realice la replicación del ADN, su transcripción a ARN, la traducción del ARN a las proteínas codificadas por dicho ADN, y que estas proteínas, a su vez, repliquen el ADN inicial; mientras que el laboratorio de Margarita Salas, es el que ha proporcionado la gran mayoría del conocimiento sobre ese sistema de replicación del ADN.
Se han descrito muchos métodos en los que se realiza simultáneamente transcripción y traducción, con lo cual, la clave era el sistema de replicación del ADN. Una de las maquinarias de replicación de ADN más simples, mejor descritas y a la vez más eficientes, es la del virus bacteriano Phi29, de genoma lineal protegido por proteína terminal.
La colaboración entre los dos equipos, permitió al laboratorio del doctor Danelon utilizar ventajosamente la maquinaria de replicación de ADN de Phi29. Este equipo, optimizó una reacción de transcripción-traducción de modo que, al añadir a dicha reacción un minigenoma lineal que codificaba las proteínas esenciales para la replicación del ADN de Phi29, dichas proteínas eran producidas e inmediatamente empezaban a trabajar sobre el minigenoma que las codificaba haciendo copias del mismo, con lo cual se podía considerar cerrado el ciclo.
“Pero no solo eso, sino que se comprobó que, a su vez, los nuevos minigenomas producidos eran perfectamente funcionales y, en presencia de los componentes adecuados, volvían a producir las proteínas de replicación y a ser nuevamente replicados”, describen los autores del trabajo. “Además, llevamos a cabo este tipo de ciclo tres veces sucesivas, purificando los mini-genomas y transfiriéndolos a nuevas reacciones que aportaban todos los componentes necesarios, menos las proteínas de replicación”, añaden.
Para aproximar más la dirección del trabajo hacia la meta de una célula sintética, el laboratorio del Dr. Danelon incluyó la reacción completa descrita en los liposomas que simulaban la membrana celular. Así, se observó que, de nuevo, la reacción se llevaba a cabo, se producían las proteínas de replicación y éstas replicaban el ADN.
Aun cuando falte todavía mucho camino para conseguir una célula que viva, crezca y se divida en células hijas, este trabajo supone un paso decidido en esa dirección. Además de replicar el material genético, el método permitiría incorporar nuevas funciones, como la producción de membrana, división celular, obtención de energía, metabolismo, etc.
Estas funciones se incorporarían como módulos de ADN que codificarían las proteínas correspondientes y que se irían añadiendo al minigenoma que se replica inicial, para hacerlo más parecido a una célula. Otra de las funciones que se podría incluir, es la evolución darwiniana basada en mutaciones y selección de los individuos mejor adaptados.
